2. SO SÁNH QUY TRÌNH TÌM NGUỒN THUỐC CHỨNG
2.3. Xác định chiến lược cung ứng sẽ được sử dụng
2.3.1. Lựa chọn và liên hệ nguồn thuốc chứng cho một thử nghiệm lâm sàng
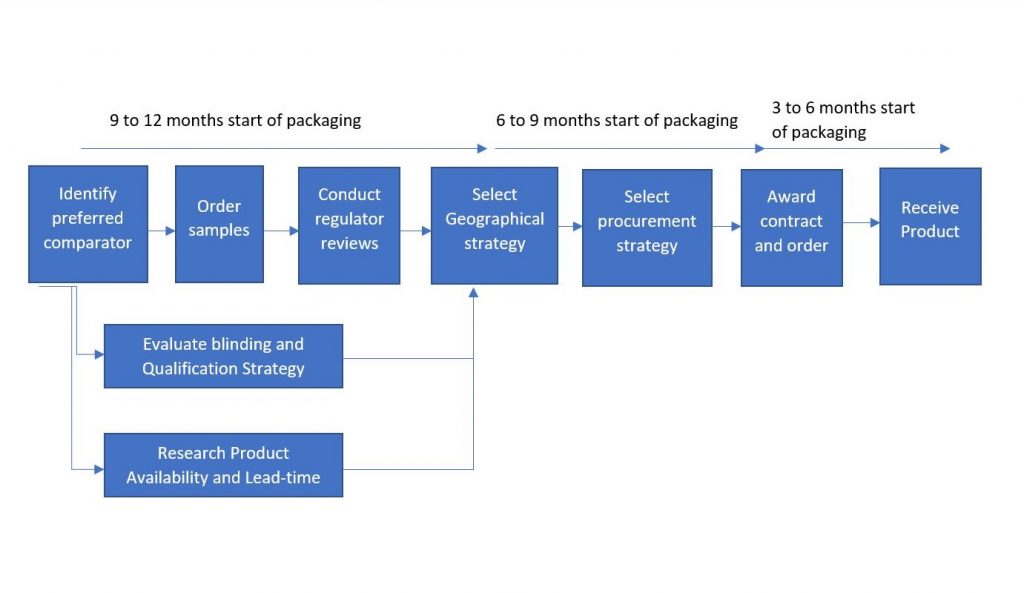
Quá trình tìm nguồn cung cấp thuốc chứng nên bắt đầu khoảng 9-12 tháng trước khi nhận được thuốc chứng. Điều này sẽ cho phép dự phòng và xác định được phương án chiến lược tốt nhất trong suốt thời gian thử nghiệm.
Xác định thuốc chứng ưu tiên
Thông thường, việc xác định đối tượng thuốc chứng ưu tiên là trách nhiệm của các nhà nghiên cứu lâm sàng và chuyên gia y tế, nhưng các bộ phận tiếp thị marketing cũng có thể tham gia. Các cá nhân từ các bộ phận này nên làm việc cùng nhau để xác định thuốc chứng mục tiêu. Bộ phận tìm nguồn cung ứng thuốc chứng đối chiếu và phản hồi dữ liệu để có thể đưa ra quyết định sáng suốt trên thuốc chứng tốt nhất.
Yếu tố liên quan đến việc đưa ra quyết định về thuốc chứng bao gồm những cân nhắc quan trọng sau:
- Tính nhất quán của thuốc chứng trên thị trường mà IMP sẽ được so sánh
- Tính khả dụng và khả năng tiếp cận sản phẩm
- Rủi ro cung cấp
- Chi phí
- Dễ làm mù
- Tuân thủ các yêu cầu quy định
Trong thử nghiệm có kiểm soát, các biến phải được giữ nguyên, ngoại trừ một biến đang được thử nghiệm. Tính nhất quán của thuốc chứng cần được xem xét, đặc biệt khi đưa ra bất kỳ tuyên bố nào chống lại thuốc chứng, đây thường là mục tiêu của các thử nghiệm như vậy. Ví dụ, nếu có một loạt các hàm lượng của thuốc chứng có sẵn trên các thị trường khác nhau, tổ chức mua hàng có thể chọn hàm lượng của thuốc chứng xuất hiện thường xuyên nhất hoặc có thể chọn loại bỏ một số biến có vấn đề khỏi nghiên cứu, tùy thuộc vào mục tiêu của nghiên cứu và tầm quan trọng của thị trường đó.
Các lô sản phẩm cần cùng 1 lô để có thể giúp duy trì tính nhất quán và tạo ra hiệu quả. Cần tránh tìm nguồn cung ứng nhiều lô từ một hoặc nhiều nhà cung cấp để tích lũy đủ nguyên liệu.
Một tổ chức mua hàng có thể xây dựng một bản mô tả về những gì có sẵn ở mỗi lãnh thổ bằng cách xác định các hàm lượng, công thức, cách trình bày và thương hiệu khác nhau sẵn có. Một dấu hiệu ban đầu có thể được thiết lập về mức độ dễ dàng sẵn có của mỗi lựa chọn, cho phép xây dựng chiến lược.
Tính khả dụng (thời gian thực hiện, giấy phép và ngày hết hạn) và quyền truy cập cần được xem xét. Tính khả dụng và khả năng tiếp cận đều góp phần vào rủi ro liên quan đến việc tìm nguồn cung ứng nguồn thuốc chứng.
Khi một số thuốc chứng tiềm năng đã được xác định, các mẫu thử phải được đặt hàng để chúng có thể được kiểm tra. Có thể đánh giá khả năng xảy ra biến đổi nào trong làm mù, ví dụ, bao nang hoặc đóng gói lại. Để biết thêm thông tin về việc sửa đổi và cân nhắc độ ổn định. Việc cân nhắc cuối cùng là đánh giá các chi phí tiềm ẩn của một chiến lược tìm nguồn cung ứng và để cân bằng những chi phí này với những rủi ro đã xác định và các lựa chọn có sẵn.
Chọn thuốc chứng branded or generic
Việc lựa chọn sử dụng thuốc chứng branded or generic có thể là một sự cân nhắc về chi phí. Nó cũng có thể được xác định dựa trên các yếu tố như:
- Sự hiện diện và trạng thái của các loại thuốc tốt nhất trên thị trường
- Các nhu cầu chưa được đáp ứng và phân khúc thị trường
- Định giá của thuốc chứng trên thị trường
- Nhận thức được những ưu điểm khác biệt của thuốc nghiên cứu về mặt hiệu quả và / hoặc hồ sơ an toàn
Việc lựa chọn một thuốc generic làm sản phẩm thuốc chứng có thể bị loại trừ trước khi có thể xem xét lợi thế về chi phí. Việc sử dụng một branded có thể là cần thiết để đáp ứng các mục tiêu thương mại của một nghiên cứu.
| Lựa chọn | Branded | Generic |
| Ưu điểm | Thường tốt nhất để làm thương mại | Rẻ hơn |
| Có thể là lựa chọn duy nhất theo tiêu chuẩn chăm sóc | Dễ có chứng từ | |
| Đã được chứng minh với dữ liệu lâm sàng / phi lâm sàng có sẵn | Các nhà sản xuất có thể sẵn sàng cung cấp các hoạt chất cùng với giả dược | |
| Nhược điểm | Mắc hơn | Phải chắc chắn lấy hàng từ một nguồn tin cậy (mặc dù điều này cũng áp dụng cho branded) |
| Có thể nhạy cảm về mặt thương mại, tức là, truy cập số lượng lớn có thể thu hút sự chú ý đến hoạt động thử nghiệm | Chất lượng sản phẩm có thể không được công nhận ở tất cả các vùng lãnh thổ (chất lượng cũng có thể là một vấn đề với branded) | |
| Có thể khó khăn hơn khi tiếp cận số lượng lớn ở tất cả các lãnh thổ nghiên cứu | Hàm lượng, cách trình bày hoặc công thức ít có khả năng có sẵn ở tất cả các lãnh thổ được nghiên cứu |
Đặt hàng mẫu
Khi thuốc chứng đã được chọn, tổ chức mua hàng có thể đặt một mẫu sản phẩm để đánh giá nội bộ. Các mẫu có thể tạo cơ hội để nghiên cứu nhãn và tờ rơi thông tin bệnh nhân và tiến hành kiểm tra độ ổn định.
Các nhãn cho sản phẩm được phê duyệt ở Châu Âu có thể được tìm thấy trên các trang web của EMA.
Các mẫu cũng cho phép đánh giá cách đóng gói, khả năng làm mù và cũng như đánh giá chất lượng để có thể bắt đầu phát triển.
Tránh hàng giả
Thuốc giả gây rủi ro cho sự an toàn của bệnh nhân do:
- Không chứa đúng số lượng hoặc chất lượng của hoạt chất
- Không chứa bất kỳ hoạt chất nào
- Có thể chứa tác nhân có thể gây hại trực tiếp cho bệnh nhân.
Khi tìm nguồn cung cấp thuốc chứng cần biết được khả năng truy xuất nguồn gốc của sản phẩm. Tổ chức mua hàng hoặc nhà cung cấp trực tiếp của họ phải có khả năng truy xuất nguồn gốc thuốc trở lại nhà sản xuất và giảm thiểu nguy cơ bất kỳ loại thuốc giả nào xâm nhập vào chuỗi cung ứng.
An toan trong chuỗi cung ứng có thể đạt được bằng cách lấy thuốc chứng trực tiếp từ nhà sản xuất, nhưng điều này hiếm khi có thể thực hiện được do thiếu thông tin liên hệ và những lo ngại về tính bảo mật. Mục tiêu phải là giữ cho chuỗi cung ứng càng ngắn càng tốt, tốt nhất là chỉ nên có một mắt xích trong chuỗi (tức là một nhà cung cấp) giữa tổ chức cần mua hàng và nhà sản xuất. Nếu có thể, nên sử dụng các phần bổ trợ đã được kiểm toán để:
- Có thể cung cấp tài liệu để xác định chất lượng của thuốc được cung cấp
- Có một quy trình phục hồi để ghi lại khả năng truy xuất nguồn gốc của một thuốc chứng
Nguồn: ISPE Good Practice Guide





You must be logged in to post a comment.